Химические свойства ароматических углеводородов
Химические свойства ароматических углеводородов
1. Реакции электрофильного замещения
2. Механизм электрофильного замещения
3. Реакции присоединения
4. Реакции окисления
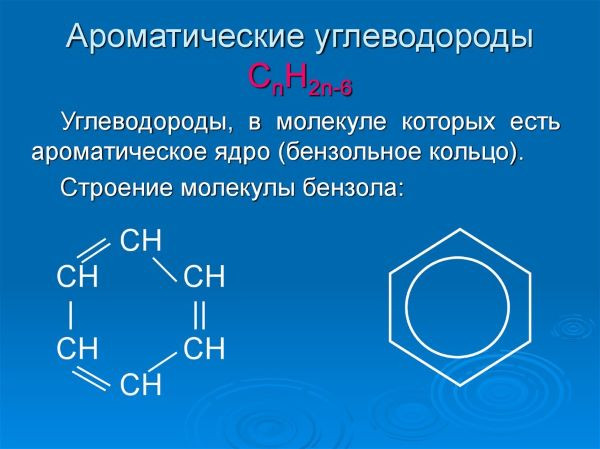
Присутствие 6π-электронной сопряженной системы на прямую влияет на химические свойства бензола и его производных. Ароматический цикл сохраняется у аренов в реакциях электрофильного замещения. Реже встречаются реакции присоединения, в результате которых нарушается ароматичность цикла. Исключительно жесткие условия могут привести к тому, что арены поддаются им и вступают в окислительные реакции.
Реакции электрофильного замещения
Они представляют собой особую группу реакций, которые в наибольшей степени характерны для аренов.
Примеры реакций:
- Галогенирование. При наличии катализаторов галоген замещает атом водорода в бензольном ядре. Оптимальная температура, при которой протекает реакция – от 15 до 25 градусов. С помощью этого метода можно извлечь ароматические галогенпроизводные.
- Нитрование. В данном случае показано применение нитрующей смеси. В её состав входит концентрированная азотная и серная кислота. Воздействие исключительно азотной кислоты также приводит к нитрованию бензола, но гораздо медленнее.
- Сульфирование. Применение высокоактивной серной кислоты приводит к образованию бензолсульфоновой кислоты. В данном случае наблюдаем как сульфогруппа вытесняет атомы водорода.
Механизм электрофильного замещения
Первый этап. Появляется неустойчивый π-комплекс, перетекающий в ϭ-комплекс. При этом нарушаются ароматические системы, 1 атом углерода переход в гибридное состояние. Энергичной фазой реакции выступает процесс формирования ϭ-комплекса.
Второй этап. Наличие активных нуклиофилов привод к отщеплению протонов, наблюдается востонавление катализаторов. Используя энергетическую диаграмму, можно изучить механизм реакций электрофильного замещения. Химические реакции электрофильного замещения закономерно и вполне оправданно относятся к реакциям второго порядка.
Реакции присоединения
Реакции этого типа у аренов встречается редко, для их протекания необходимо наличие жестких условий.
Реакции окисления
Как правило, сильные окислители не оказывают особого влияния на химические свойства аренов. Только в присутствии катализатора и возможного протекания реакции. По сравнению с предыдущим примером гомологи бензола способны к более активному окислению.
Окисление гомологов бензола – основные характеристики:
- Вся цепь способна окислиться до карбоксильной группы, даже при наличии длинной боковой цепи.
- Если присутствует несколько боковых цепей окисление новой цепи возможно только в более агрессивных условиях (при наличии катализатора).
